■行政トピックス
1.中医協費用対効果評価等合同部会 12月20日
本格導入は見送り、支払い意思額調査でつまずき
厚労省は12月20日の中医協費用対効果評価専門部会などの合同部会に、「試行的導入における取り組みおよび制度化に向けた主な課題について」を提示した。同省が目指した18年度の「制度化(本格導入)」は見送りとなったが、18年4月に「試行的導入」における13品目(うち医薬品7品目)の費用対効果評価結果に基づく価格改定を実施し、それを踏まえて、「制度化」に向けた検討を続け、18年度中に結論を得ることが盛り込まれた。
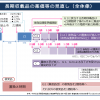
試行的導入は、16年4月に対象品目が選定され、5月から企業分析について分析手法等に関する事前相談を開始、9月には費用対効果評価専門組織において分析枠組み等の妥当性を確認し、10月から企業分析が開始された。17年4月に企業分析の結果が提出され、5月から同専門組織による再分析がスタート。10月に再分析結果がまとまり、年内の総合評価(アプレイザル)を経て、18年4月に価格調整が行われる段取り。
ただ、決して順調に進んだわけではなく、同省が目指した18年4月の「制度化」は断念。「試行的導入」対象品目の価格改定を行うことで同省は何とか面目を保った格好だ。難航を決定的にしたのが、一般人を対象とした「支払い意思額調査」の実現性。調査票が、一般人に対して、完全に健康な状態で1年間だけ寿命を延ばすことができる治療法に対して、公的医療保険から支払える額を問う内容だったため、「国民は公的医療保険というものをあまり理解していない」(幸野庄司健保連理事)など、中医協委員から疑問の声が噴出。
同省は「支払い意思額調査」の実施を棚上げ。「試行的導入」に意思額調査結果の活用を断念し、過去に実施された調査結果(2010年の白岩らによる調査)および英国における評価基準で代用した。
したがって、「支払い意思額調査」の実施は、今後の制度化に向けた大きな検討課題の一つ。12月20日の合同部会で、吉森俊和委員(協会けんぽ理事)は、試行的導入で参照したデータが約10年前の調査結果であることを踏まえ、「当時の経済状況、社会情勢、また近年の高額薬剤の登場による医療の高度化の進展に鑑みて医療環境が大きく変わってきていることから、国民の考え方も変化していると思われる。制度化の検討に当たって最低限1回は支払い意思額調査を行うべき」と主張。
一方、松本純一委員(日医常任理事)は「試行的導入時に基準値を設定したが、不都合があったため、何か新たな基準値を設定しなければならないということであれば、その際に議論すべきだが、このままでは支払い意思額調査の実施は駄目である」と主張した。
試行的導入、2段階対応品目も
過去に行われた調査結果(2010年の白岩らによる調査)を参照し、さらに英国における評価基準を参考にして合同部会で決まった基準値が500万円。つまり、試行的導入の対象となった13品目の科学的検証をICER(増分費用効果比)を用いて行い、これに倫理的・社会的影響の検証を加味して、計算した値が500万円以上となった場合に価格引き下げ調整が行われることが決まった。
ただ、試行的導入において、「一部の品目につき、企業分析の結果と再分析の結果が大きく異なることが分かった」(11月10日の合同部会で古元重和医療課企画官)ことから、この品目に限っては、価格変動のより少ない分析結果の方を採用して、4月に価格調整をいったん行い、その後、妥当性の高い分析のあり方について検証作業を進め、最終的な価格調整を行うという2段階で対応することになった。
両分析結果が大きく異なったのは、企業分析を開始する前に、分析の枠組み等に関する事前相談を行った上で進めたものの、それでも互いの認識の違いや、より適切なデータについての見解の相違が残ったままだったことが要因とされた。
12月20日の合同部会では、松本純一委員は「そのような間違いがあったため、それを検証して制度化に向けてということと理解するが、試行的導入に対して考え方が甘かったのではないか。今後の検証結果を待ちたい」と述べた。吉森委員は「実際に両分析結果の価格差異が大きくなった品目について、どの程度の価格調整が行われたのかを含め、試行13品目の調整結果についてきちんと整理して、納得感のあるように開示してほしい」と要望した。
なお、厚労省が示した18年度中に結論を得る「制度化に向けた検討課題」は以下の通り。
(1)対象品目の選定
・費用対効果評価の対象とする品目の範囲
・選択基準(補正加算、市場規模等)
・除外基準
・品目選定のタイミング
・対象品目の選定および公表の手続き等
(2)企業によるデータ提出
・分析前協議(事前相談)の方法
・分析にかかる標準的な期間の設定
・分析ガイドラインのあり方
・費用対効果評価専門組織等のかかわり等
(3)再分析
・分析にかかる標準的な期間の設定
・第三者的視点に立った透明性の高い組織・体制のあり方
・費用対効果専門組織等のかかわり等
(4)総合的評価(アプレイザル)
・科学的観点からの検証方法
・倫理的、社会的影響等に関する考慮要素
・評価結果のとりまとめ方
・評価結果の報告、公表の仕方
・第三者的視点に立った透明性の高い組織・体制のあり方等
(5)価格調整
・価格調整の対象範囲
・価格調整率
・価格調整にかかる基準値の設定(支払い意思額調査を含む)
・価格調整係数
・価格調整のタイミング等
(6)分析結果が大きく異なった品目への対応
・事前相談の充実
・より妥当性の高い分析方法の検討
・臨床の専門家からの意見聴取等
2.偽造品流通防止に関する検討会 12月20日
最終とりまとめ報告書を公表
医療用医薬品の偽造品流通防止のための施策のあり方に関する検討会は12月20日に最終とりまとめ案を大筋で了承。28日に厚生労働省のウェブサイトで最終とりまとめ報告書を公表した。検討会では10月から最終とりまとめに向けて ▽流通過程における品質の確保などに向けた検討 ▽規制の法令上の位置付けのあり方の検討―を中心に議論していた。
最終とりまとめ報告書では、流通過程における品質確保に向けて、「偽造医薬品を含め品質の疑わしい医薬品を漏らさず検知する体制を整備することが求められる」と強調した上で、そのためにPIC/SのGDPガイドライン全般に準拠した国内向けGDP ガイドライン(グッド・ディストリビューション・プラクティス、医薬品の適正流通基準)を作成し、厚労省が広く周知し、卸売販売業者の自主的な取り組みを促すよう求めた。厚労省医薬・生活衛生局総務課の紀平哲也室長によると、国内向けGDPガイドラインは17年度中に作成し、18年度中に公表する見通し。12月20日の検討会後、紀平室長は「研究班で作業を進めていて、今年度の研究成果として作成され、それを受けて厚労省の方で来年度出す方向だが、来年度のいつかは今の状況ではっきり話すのは難しい」とした。
また、最終とりまとめ報告書では「卸売販売業者の業務を行う体制に関する許可基準として、例えば、業務手順書の作成と手順書に基づく業務の実施などを追加することについて、制度全体の課題としてさらに検討を進め、できるだけ早く許可基準として位置付けるべきである」と提言。加えて、薬局開設者と管理薬剤師の責務に言及し、特に「薬局開設者への罰則のあり方を含めて制度全体の課題としてさらに検討を進めるべきである」とした。これら検討事項は、厚生科学審議会の医薬品医療機器制度部会で議論される。
3.未承認薬・適応外薬検討会議 12月22日
ジアグノグリーンなど2製品が公知と判断
第33回医療上の必要性の高い未承認薬・適応外薬検討会議は12月22日、日本外科学会などが要望した第一三共の蛍光血管造影剤ジアグノグリーン(一般名インドシアニングリーン)の「血管及び組織の血流評価」の効能・効果と、小児腎臓病学会が要望した田辺三菱製薬の抗サイトメガロウイルス化学療法剤バリキサ(バルガンシクロビル塩酸塩)の「サイトメガロウイルス感染症のリスクのある小児(固形臓器)移植後のサイトメガロウイルス感染予防」の効能・効果について医学薬学上公知であると判断した。今後、審議会の評価を経て、公知申請される。ジアグノグリーンは脳神経外科手術時における脳血管の造影の効能・効果で承認されているが、「個別の部位の血流の測定ということで何度も要望があり、そろそろまとめたほうがよかろうということで個別で挙がっていたものをまとめて、血管及び組織の血流評価として複数の臓器で使っていただけるようにした」(公知申請の妥当性を評価した循環器ワーキンググループ)。バリキサは成人に対する臓器移植(造血幹細胞移植を除く)におけるサイトメガロウイルス感染症の発症抑制の効能・効果で承認されており、これを小児適応に拡大するもの。現在、小児への投与に適した剤形としてドライシロップ剤の開発が進められている。
また、検討会議は日本皮膚科学会が要望したマルホとガルデルマのメトロニダゾール(一般名)の「酒さの炎症性皮疹並びに紅斑」の効能・効果と、日本造血細胞移植学会が要望したクリニジェンのホスカルネットナトリウム水和物(一般名)の「造血幹細胞移植後ヒトヘルペスウイルス6脳炎」に対する効能・効果は医療上の必要性が高いと判断された。今後、企業に開発要請がなされ開発が進められる。
日本老年精神医学会が要望した軽度および中等度のアルツハイマー型認知症(AD)患者にドネペジル塩酸塩(一般名)の1日10㎎投与を可能とする用法・用量の変更と、日本産科婦人科学会が要望したエプタコグアルファ(一般名)の重篤な産科危機的出血に対する効能・効果は医療上の有用性に該当しないと判断された。
■記者会見
1.革新性「社会全体の議論がいま必要」
-ファイザー日本法人:原田明久社長-
ファイザー日本法人の原田明久社長は12月13日の記者懇談会で社長就任の挨拶を行い、「医療におけるイノベーションは産官学それぞれが単独で生み出すものではなく、患者を含めた4者が連携を強めて社会全体で生み出していくものと考えている。それを理解した上で革新的医薬品とはどのようなものか、社会全体の議論がいま必要ではないか」と指摘。ファイザーとして「たんに治療だけでなく、病気を背負っている患者の生活の質にポジティブなインパクトを与えるペイシェントヘルスを目指している」とした上で「そこで使われる薬剤の価値も患者にどれだけインパクトを与えることができるかということが重要で、これが世界に通用する革新的医薬品の1つの価値基準ではないかと考えている」と述べた。
会には梅田一郎名誉会長も登壇し、09年12月からの社長在任8年間を振り返り、「新薬を開発しても好調であれば再算定を受けるということで会社の成長は思うに任せなかったが、社員が脇を引き締め、大いに生産性を向上させてくれた」と語り、「全社禁煙の取り組みは私自身の思い入れもあり印象に残っている。社長就任時に15%だった社員の喫煙率は昨年4.8%まで低下し、今年はさらに下がっていると思う。20年までに社員の喫煙をゼロにすることを目指している。それが達成されるよう今後も陰ながら応援したい」と話した。