■セミナー便り
1.イブランスは「ゲームチェンジャー」
-昭和大学乳腺外科学:中村清吾教授-
新規メカニズムの乳がん治療薬イブランス(パルボシクリブ)の発売を前に、ファイザーは11月20日、都内でプレスセミナーを開いた。昭和大学乳腺外科学の中村清吾教授と愛知県がんセンター中央病院の岩田広治副院長兼乳腺科部長が講演し、進行乳がんの治療がパラダイムシフトを迎えていることを紹介した。
同剤は、細胞周期の調節に主要な役割を果たすサイクリン依存性キナーゼ(CDK)4/6を阻害する。中村氏によると、海外では乳がん治療の「ゲームチェンジャー」と受け止められているという。
国内の統計では、Ⅳ期乳がん患者の5年生存率は30%台半ばだが、他のがん種よりは長期生存が期待できる。中村氏は「がんによる症状を抑え込み、自分らしく生きることが可能だ」とし、そこに様々な薬物療法の役割があるとした。また、イブランスの投与対象となる「ホルモン受容体陽性・HER2陰性」の患者は乳がん全体の約70%を占めるとした上で、「生存率改善のキーポイントとなる」と期待を寄せた。
岩田氏は国際共同第3相試験「PALOMA-2」「PALOMA-3」の結果を紹介。両試験とも、主要評価項目の無増悪生存期間をプラセボよりも有意に延長した。PALOMA-2では「臨床的有用率」が84.9%で、「ほとんどの患者は腫瘍が増大せず、がんとともに生きることが可能だ」と述べた。副作用として好中球減少症が最も多く認められたが、自覚症状はほとんどなかったという。
その上で、臨床使用の例として、閉経後乳がんの再発後の1次治療にレトロゾール(ホルモン療法薬)+イブランスを、2次・3次治療にフルベストラント(同)+イブランスを挙げた。一方、「効能・効果からはレイトラインで使用することもできるが、そのような患者に、本日紹介した臨床試験と同じ効果が得られるわけではない。臨床家が使い方を間違えないように啓発することが重要だ」と指摘した。
■セミナー便り
2.C型肝炎治療薬「究極まで来た」
-虎の門病院:熊田博光分院長-
虎の門病院の熊田博光分院長は11月28日、アッヴィ合同会社主催のC型肝炎治療薬マヴィレットのセミナーで「C型慢性肝炎・代償性肝硬変の治療は著しく進歩し、究極まで来た」と語った。同剤の特長として、ジェノタイプ問わず同一レジメンで最短8週間の治療が可能な点を挙げた。
国内第3相試験(CERTAIN-1試験、同-2試験)の結果を示し、1型はY93やL31の薬剤耐性変異にも高い効果が期待できると紹介。「これまで1回治療に失敗すると耐性が増えて治らなくなると言われていたが、今回はその理屈が通らなくなって耐性が3つ、4つ、5つでもみんな治る」と言う。2型はリバビリンと併用する必要がなく、貧血合併例や腎障害の患者に適応可能であり、特に2型の重度の腎機能障害合併例に対して有効性が期待されるとし、「ソバルディ(+リバビリン)が使えなかった人にも使える」と述べた。
マヴィレットの上市を受けて熊田分院長は「これでファーストラインの薬剤の開発は終わる」と強調。「これからは治った後にがんにならないようにする線維化改善剤やNASH(非アルコール性脂肪性肝炎)を改善する薬剤の開発に移っていく」と見通しを示した。
■セミナー便り
3.SLEの新薬開発は難しい
-慶應義塾大学リウマチ・膠原病内科:竹内勤教授-
全身性エリテマトーデス(SLE)の患者から「関節リウマチのような生物学的製剤はないのですか」と何回聞かれたかわからない-。慶應義塾大学リウマチ・膠原病内科の竹内勤教授は11月28日に行われたグラクソ・スミスクラインのメディアセミナーで、SLEの新薬開発の困難さをこのように述べた。
SLEは代表的な膠原病かつ自己免疫疾患で、20~40歳代の女性に好発する。皮膚の発疹、発熱、倦怠感、関節痛・筋肉痛、蛋白尿などの症状・臓器障害を呈する。寛解と再燃を繰り返して慢性に経過する。治療はステロイドが中心で、寛解導入に用いた後も、寛解維持に一定量を継続する。そのため、「ステロイドの長期投与による臓器ダメージが蓄積し、圧迫骨折などでQOLも低下する」(竹内氏)。そこで、ステロイド以外の薬剤を併用してステロイドを減量しつつ寛解を維持することがポイントだと指摘した。
そうした中、同社のベンリスタ(ベリムマブ)がSLEに対する初めての生物学的製剤として今年9月に承認された。B細胞の分化に寄与する可溶型Bリンパ球刺激因子(BLyS)を標的とする抗体薬で、SLEに特徴的な自己抗体の産生を抑える。
竹内氏によると、いくつかの生物学的製剤がSLEに開発されていたが、第3相試験で有効性を証明できなかった。SLEの多彩な臨床症状をすべてとらえて評価することが困難なためだという。一方で、ベンリスタの成功要因の1つに、SLEの活動性を評価する新しい指標(SRIレスポンダー率)を初めて用いたことを挙げた。
同剤の位置づけとしては、ステロイドでコントロールできない重症患者や活動性が残存する低~中活動性患者における寛解導入、あるいはステロイドの減量困難例に用いるとした。国内導入が遅れていた世界標準薬ヒドロキシクロロキン(HCQ)との使い分けについては、「HCQは基礎薬として用い、再燃したときにベンリスタを用いる」と述べた。
■セミナー便り
4.循環器医も糖尿病に関心「連携で良い治療可能に」
-トロント大学医学・栄養学:L・A・レイター教授-
「幾つかの血糖降下薬が心血管イベントのリスクを低減させることが分かり、心臓専門医も血糖コントロールの重要性を理解するようになった」。そう語るのはトロント大学医学・栄養学のローレンス・A・レイター教授。糖尿病に関するACCORD試験やADVANCE試験などに試験責任医師として参加した人物だ。世界各国でも心臓と糖尿病の専門医が連携して治療する考え方が出てきたとして、「連携を深めることで良い治療が可能になる」と述べた。
一方、国内はどうかと言えば、サノフィ糖尿病・循環器メディカル本部循環器領域メディカル部の宇野希世子部長が「循環器の先生が糖尿病に関心を持って何かできないかと考え始めているし、糖尿病の学会でも循環器のセッションが出来て、議論を一緒に行う流れが出てきている」と説明。サノフィでも16年に糖尿病領域と循環器領域を1つのビジネスユニットに統合した。その意義について宇野部長は「(SGLT2)アプルウェイと(PCSK9)プラルエントを別々に持っていってお互いのことを知らないというのは理に適わない」と指摘。「一緒に疾患として見て、先生方のヘルスケアパートナーになるという意味では理に適うようになってきた」と話した。
講演ではレイター教授も宇野部長も糖尿病患者における心血管イベント抑制に向けた脂質管理の重要性を話し、糖尿病患者を対象としてプラルエントの有効性と安全性を評価したODYSSEY DM-INSULIN試験と同-DYSLIPIDEMIA試験などを解説した。
■学会便り
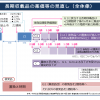
1.薬剤疫学データベースの今後の課題について議論
第23回日本薬剤疫学会学術総会
11月18日、19日に日本薬剤疫学会学術総会が東京大学 伊藤国際学術研究センターで開催された。
シンポジウム1「生物統計と薬剤疫学の専門家の人材育成」において、中外製薬の青木事成氏は多くの製薬企業は薬剤疫学等の専門力は乏しいところに、SOP研修などに多くの時間を要していると現状を述べた上で、11年1月に4人で疫学グループが発足して現在は6人体制となり、これまでに疫学の社内研修を実施し、また他部署への出張サービスなど疫学的サポートに努めている取り組みを紹介した。さらにグループ員には社内抄読会の実施や、社外研修会への参加により研鑽を積ませている。医療データを実際に活用した5つの論文を投稿しており、今後は後進に対する継続した教育が必要であると結んだ。
総合討論において生物統計と薬剤疫学ではどのようなバックグラウンドの人材を望むかとの座長の質問に対して、東京大学松山裕氏、京都大学佐藤俊哉氏、中央大学大橋靖雄氏、青木事成氏、NPO日本医薬品安全研究ユニット 久保田潔氏の5人のシンポジストは、総じて多様な背景の人材を期待し、コミュニケーション力があってチームの和を保てる人物を求めるとした。大橋氏はパブリックヘルスに対して先行期待があるものの、現在実施中の日科技連のBIOS研修では研修者にキーオープン経験者は不在であり、教育の見直しが必要であることも指摘した。次に教育体制の課題は何かとの座長の質問に対しては、青木氏はアカデミアに期待するとのことだったが、他のアカデミアのシンポジストからは大学はまだまだ教育できる者と経験が足りないとの発言があり、大橋氏は生物統計家の方は十分に供給できたが、薬剤疫学家とHTAの専門家が不足しており、またCROでは薬剤疫学を教育できる者は少ない現状を述べた。
シンポジウム4「改正GPSP省令下における市販後医薬品のリスクとベネフィットの評価」でPMDAの澤田想野氏は改正までの経緯を示し、これまでの調査の限界と欧米の薬剤疫学的手法の発展とMID-NETの開発により市販後医薬品の評価にデータベースの利用を可能にしたとし、PMDAはチームとして計画書に最初から関与していくと述べた。また座長のPMDA石黒智恵子氏からMID-NETの料金に多少の誤解があるとして、1品目何テーマでも8年間で4200万円ほど、集計表のみでは1000万円ほどであるとの補足説明があった。
浜松医科大学の川上純一氏はデータベースは万能ではなく研究者の育成が必要とし、院内薬局と近隣病院薬局と連携して、ニューキノロン製剤は腱障害のリスクが高いことや白金製剤の聴覚障害は製剤間で大きな違いはないことの安全性情報を発信して成果を挙げたことを強調した。
武田薬品工業の宮川功氏は自社の安全情報に対する取り組み状況を述べた。承認申請の第3相までと承認後の第4相はリスクマネジメントとして一連のものと位置付けると、第2相では特殊検査も可能であるという。また小児に対する調査は製販後だから実施できるとした。また、それぞれの段階で検出できる副作用のタイプ(A,B,C)は異なり、タイプ別副作用を検出して、特定リスクを最小化し、潜在リスクを減少させることが目標であるとした上で真実を掴み真実に近づくことが必要であると強調した。一方で、安全性評価レポートのテンプレートの有無は企業ごとに異なる現況を紹介した。
総合討論では、使用成績調査において倫理委員会審査、同意、対価などについての議論があったが、フロアから元製薬企業の開発担当者の意見として、審査結果によってはこれまでの商品が販売できなくなるリスクがあり、データ不正の温床にもなりかねない懸念があるとの発言があった。これについて澤田想野氏は単一のデータベースだけで判断するものではなく、懸念があったら計画時に検討する上に、医療経済性評価やその他の多くの調査から総合判断するとコメントした。
今回の学術集会において、GPSP改正によって使用成績調査に代わり科学的なアプローチが可能となることを歓迎するが、薬剤疫学研究実施の前提としてデータベースの整備とそれに関わる研究が必須であることが多くの演者から述べられた。データベース研究の恣意性などは今後の課題もあり、各種存在するデータベースとそれを活用する研究者に対して過大に期待されている面もある。Big Dataを真のKnowledgeとするためにはまだ克服すべき多くの課題がある。