■行政トピックス
1.中医協費用対効果評価専門部会 6月28日
保険償還可否の判断には当面用いず
中医協費用対効果評価専門部会は6月28日、今夏の中間報告取りまとめに向け、「対象品目の選定のあり方」および「費用対効果評価の反映方法」をテーマに議論し、厚労省の提案内容を大筋で了承した。ただ、評価結果を保険償還の可否の判断に用いることについて、幸野庄司委員(健保連理事)が「可能性を排除しない方が良いのではないか」と述べたのに対し、松原謙二委員(日医副会長)が「有効性・安全性が確認されたものは保険償還されるという前提で、国民に信頼されているということをもう少し重く受け止めてほしい」とかみつく場面もあった。
対象品目について厚労省は、医療保険財政への影響度を重視する観点から、新規収載品および既収載品ともに要件として、1.革新性が高い品目(補正加算のある品目等) 2.市場規模の大きな(市場規模が一定程度を超える)品目-の両方を満たすこととしてはどうかと提案。ただ、市場規模が一定程度を超えない場合であっても、著しく高額な品目等について、薬価算定組織の意見等を踏まえ柔軟に対応する方向性を明示。また、効能追加等により収載後に一定額以上拡大したものも対象としてはどうかと提案した。
一方、評価の反映方法については、これまでの議論で、保険償還の可否の判断に用いることに慎重意見が大勢を占めたことから、「原則として償還の可否の判断には用いず、価格の調整に用いる位置付けにしてはどうか」とし、その上でドラッグ・ラグを生じさせないため、一度、薬価を設定して保険適用し、後から、費用対効果評価の結果を用いた価格調整を行う方法が考えられるとした。
診療側は厚労省案に概ね賛同。一方、支払側からは、保険償還の可否の判断に用いることについて「まずは薬価収載後の価格調整に用いることでよいと思うが、今後この制度が安定的に運用され、評価の期間が短縮され、この制度の実効が表れてくるタイミングでは、保険収載の可否の材料として用いることも検討していいのではないか」(吉森俊和協会けんぽ理事)、「当面は価格調整のみに用いることで進めていけばよいと思うが、未来永劫そうではなく、ある程度この制度が定着し、数値が正確になった際には、例えば高額な医薬品について、保険収載の可否の判断に用いる可能性を排除しない方が良いのではないか」(幸野委員)との見解が示された。
これに対し、診療側の松原委員は「(仮に保険収載されない場合)その治療を受けることができるのは収入の多い人や別の保険に加入している人になってしまい、皆保険の根底が崩れることになる」などと反発した。一方、吉森、幸野両委員が、価格に反映させるタイミングとして、できるだけ速やかに、年4回の新薬収載時を活用すべきだとしたのに対しては、松原委員は「年4回改定する機会があれば、データを見てその費用が高過ぎれば安くすれば済む話」と述べた。
2.中医協薬価専門部会 6月28日
厚労省、原価計算方式でのイノベ評価見直しを提案
中医協薬価専門部会は6月28日、薬価制度抜本改革に向け、「イノベーションの評価」をテーマに議論した。イノベーションの評価として、平均的な営業利益率に対して補正が行われている原価計算方式について、厚労省の中山智紀薬剤管理官は「類似薬効比較方式と比べた時に、評価があまり高くならない仕組み」との認識を示し、「正確性・透明性が確保されたものについて高く評価できる仕組みとすることは良いのではないか」と踏み込んだ。委員からは「製造経費、製造原価が中医協の場で公開できないことには納得できない」(中川俊男日医副会長)など、反発する声が上がった。
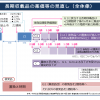
原価計算方式は、比較薬が存在せず、類似薬効比較方式で算定できない場合に用いられ、1.原材料費 2.労務費 3.製造経費 4.一般管理販売費 5.営業利益 6.流通経費 7.消費税-を積み上げて薬価を算定するもの。イノベーションに対する評価は、営業利益率に対する補正の形で行われているが、この日、厚労省が示した試算によると、営業利益率に対して20%、30%、40%の加算を行っても、薬価に対する実質加算率は3.52%、5.43%、8.91%と、5分の1程度になってしまう。
そこで、同省は「製造経費等が明確にされた場合に、より評価できるような仕組みを設け、これにより、併せて、原価計算方式における正確性・透明性を向上させることについてどう考えるか」と問題提起した。
安部好弘委員(日薬常務理事)は「類似薬効比較方式と比べてかなり評価が限定的という印象がある」と見直しに前向きな発言をしたが、ほかの委員からは「どのような費用を明らかにすることができるのか判然としなければ、それに対する評価の具体的な議論に入れない」(吉森俊和協会けんぽ理事)、「原価計算方式は積み上げ方式で、製造総原価には原材料費や研究開発費など我々には見えないものがたくさんある。ブラックボックスに加算を付けるわけには絶対にいかない」(幸野庄司健保連理事)と、支払側が慎重論を展開。
診療側からも「製造経費、製造原価がこの中医協の場で明確だな、説得力があるなという時に評価するということで良いのではないか」(中川委員)との意見が示され、中山薬剤管理官は「中医協の公開の場に正確性・透明性があるということを出していくやり方については、慎重に考えていかなくてはならない」と答えた。
■セミナー便り
1.サイラムザのバイオマーカー「9月のESMOで」
-静岡県立静岡がんセンター消化器内科:山﨑健太郎医長-
静岡県立静岡がんセンター消化器内科の山﨑健太郎医長は6月21日、日本イーライリリー主催のメディアセミナーで「大腸がんの遺伝子関連検査と治療最前線」と題して講演を行った。同社の大腸がん治療薬で血管新生阻害剤のサイラムザ(一般名ラムシルマブ)に関しては「現時点では有効性に関するバイオマーカーは同定されていない。今年9月に開催されるESMO(欧州臨床腫瘍学会)で有望なバイオマーカーが発表されると聞いている。ベバシズマブ(製品名アバスチン、中外製薬)との明確な使い分けについてもバイオマーカーが確立されるのが待たれる」と述べた。
講演では大腸がんにおけるバイオマーカー全般について解説した。山﨑医長は「切除不能進行・再発大腸がんの予後は不良だが、新しい抗がん剤の開発により生存期間中央値は飛躍的に延長している。個々の患者に最適な治療を届けるためにバイオマーカーの探索が盛んに行われているが、国内は欧米と比べてバイオマーカーの臨床導入が遅れている」と指摘した。「大腸がん診療における遺伝子関連検査のガイダンス(日本臨床腫瘍学会)がこのギャップを埋める一助になれば」と話した。
山崎医長は各国ガイドラインにおけるバイオマーカーを紹介。国内には切除不能進行・再発大腸がんに対する抗EGFR抗体の効果を予測するためのRAS検査、遺伝性大腸がんのひとつであるリンチ症候群をスクリーニングするためにミスマッチ修復機能欠損をみるMSI(マイクロサテライト不安定性)検査がある。抗EGFR抗体はKRASexon2変異例やKRASexon2以外のRAS変異例で無効であり、一方RAS野生型に絞ると有効性が上がる。こうしたことからバイオマーカーの同定により抗EGFR抗体の投与対象例を最適化している。
一方、山﨑医長は講演で大腸がんにおけるバイオマーカーの展望としてBRAF阻害剤併用療法の効果予測因子としてのBRAF V600E、抗PD-1抗体の効果予測因子であるMSI-H、抗EGFR抗体無効因子およびHER2療法効果予測因子としてのHER2を挙げ、大腸がんでも個別化医療が進むことを示した。
BRAF遺伝子変異に関しては大腸がん患者の50~10%程度いると推計されている。ASCO2017(Kopetz S,et al.:2017 ASCO #3505)でBRAF遺伝子変異陽性の大腸がんに対してBRAF阻害剤ベブラフェニブ+セツキシマブ+イリノテカン併用群とセツキシマブ+イリノテカン併用群と比較した第2相試験(SWOG S1406試験)の結果が発表され、主要評価項目の無増悪生存期間が有意に延長し、がんが増悪するリスクを52%低下させた(ハザード比0.48、95%信頼区間0.31-0.75)。山﨑医長は「BRAF阻害剤の併用療法を行うことによって通常の治療よりもがんの増悪というものを約半分リスクを下げた。それから病勢コントロール率(DCR)が通常の治療では2割だったのが、7割近くにまで増やすことができた。予後が悪いといわれた患者に対しても治療法が徐々に開発されている。実臨床に届くことは時間がかかるが非常に期待したい」と語る。
抗PD-1抗体の効果予測因子としてのMSI-Hに関してはニューイングランドジャーナルオブメディスン誌に論文があり(Le DT,et al.N Engl JMed 2015)、山﨑医長は「大腸がんは免疫療法はほとんど効果がなかった。ただ、MSI-Hの患者、欧米では5~6%、国内では2%といわれる患者に絞って使うと非常によく効く(奏効率ORR40%、DCR90%)」と言う。
5月23日にFDAがMSI-H固形がんに対してペムブロリズマブを承認したことには「分類が臓器別から遺伝子の異常別という形に変わってきている画期的な内容だ。今後、国内でも承認を申請していくと思うが、どうなっていくか注目される」とした。
HER2遺伝子変異陽性に関しては大腸がんのうち8%程度と推計される。トラスツズマブ+ラパチニブの併用療法の効果をみたHERACLES試験が報告されている。
■セミナー便り
2.ROS1肺がん治療薬ザーコリ「非常に有効性が高い薬」
-国立がん研究センター東病院:後藤功一呼吸器内科長-
国立がん研究センター東病院の後藤功一呼吸器内科長は6月23日、ファイザーとメルクセローノが共催したROS1融合遺伝子陽性の非小細胞肺がんに適応拡大したザーコリ(クリゾチニブ)に関するメディアセミナーで「非常に有効性が高い薬」と評価。「当院の患者では右の下葉にある原発性の肺がんで、肝臓に転移があるが、ザーコリを投与することで2カ月後、このがんがすっと小さくなって、肝臓の転移はほとんど分からなくなるというくらい非常に切れ味が良い」と奏功例を紹介した。
ザーコリはALK融合遺伝子陽性の非小細胞肺がん治療薬として国内承認を取得し、17年5月にROS1融合遺伝子陽性の非小細胞肺がんへの適応拡大が認められた。肺がんの国内の発症率は年間13万人といわれ、そのうちALK融合遺伝子陽性は5%、ROS1融合遺伝子陽性は1%(約1000人)と推計されている。
ROS1融合遺伝子陽性への適応拡大はROS1融合遺伝子陽性の非小細胞肺がん患者を対象とした海外第1相試験とアジア共同第2相試験を基に承認された。
アジア共同第2相試験は、日本、中国、韓国、台湾の4カ国で実施され、化学療法による前治療歴が3レジメン以下のROS1陽性かつALK陰性の東アジア人進行非小細胞肺がん患者127人(日本人26人)が登録された。コンパニオン診断薬「OncoGuide AmoyDx ROS1融合遺伝子検出キット」でスクリーニングし、ROS1融合遺伝子陽性の患者にクリゾチニブを投与した。主要評価項目の奏効率(CR+PR)は69.3%であった。後藤呼吸器内科長は「通常の化学療法の奏功割合は30%であるが、それとはレベルが違う」と言う。
同セミナーでは近畿大学医学部外科学呼吸器外科部門の光冨徹哉主任教授も講演し、Ⅳ期肺がんの化学療法の4群無作為比較試験(FACS試験、2007)によると、「20世紀の到達点として奏効率(ORR)は30%程度、無増悪生存期間(PFS)は5~6カ月、全生存期間(OS)は1年あまりであった」とした上で、「20世紀末の肺がん患者は一つのグレーのかたまりであったが、遺伝子変異によって色とりどりであることが分かって、分けて治療することで非常に大きな有効性を得ることができる。現在はEGFR、ALK、今回ROS1が承認されて、いままでの抗がん剤よりもはるかに有効な治療ができる時代になってきた」と述べた。
肺がん診療ガイドライン16年版では、Ⅳ期非小細胞肺がんの非扁平上皮がんにおいて、EGFR遺伝子変異陽性、ALK遺伝子転座陽性、ROS1遺伝子転座陽性、EGFR/ALK/ROS1陰性・PD-L1≧50%、EGFR/ALK/ROS1陰性・PD-L1<50%もしくは不明と分けて1次治療が整理されており、ROS1遺伝子転座陽性の場合はクリゾチニブ単剤を行うよう勧められている。
■セミナー便り
3.多発性骨髄腫の治療に「新横綱」
-日赤医療センター・鈴木憲史氏-
免疫調節薬を「西の横綱」とするなら、プロテアソーム阻害剤は「東の横綱」–。日本赤十字社医療センターの鈴木憲史・骨髄腫アミロイドーシスセンター長は6月20日、武田薬品工業主催のメディアセミナーで講演し、多発性骨髄腫(MM)の新薬ニンラーロ(一般名イキサゾミブクエン酸エステル)について、治療のベースとなるプロテアソーム阻害剤であり、なおかつ同クラスで初めての経口剤であることを評価した。
MMに対してプロテアソーム阻害剤(注射剤)のボルテゾミブ、免疫調節薬のレナリドミドを中心とした薬物療法が行われている。かつてはMM患者の全生存期間(OS)は約3年だったが、これらの薬剤が登場して以降、「7年程度のOSが期待できるようになり、『慢性疾患』と呼べるようになった」(鈴木氏)。とはいえ、治癒は困難であり、再発を繰り返すごとに、薬剤の有効性持続期間が短くなっていくという。
また患者は高齢者が多く、疾患の特徴として骨破壊を呈するため、通院などに要する患者・家族の負担も大きいという。既存のプロテアソーム阻害剤は、治療サイクル数にもよるが、週2回の注射を必要とする。
鈴木氏は、ニンラーロと標準治療(レナリドミド+デキサメタゾン)との3剤併用療法はすべて経口で施行できることを評価し、患者の生活スタイルや忍容性に合わせて治療が可能になると指摘した。働きながら治療することも可能になると述べた。医療機関にとっても経口剤は、関与する医療従事者の数が注射剤よりも少なくて済むことを示した。
ニンラーロの下痢、嘔吐などの消化器毒性については、減量や対症療法でマネジメントが可能であると述べた。今後の治療戦略としては、「治癒を目指す」「治療を継続してコントロールする」「苦痛の少ない治療を提案する」の3つの方向性を示した上で、患者と医療従事者がともに考える時代になると指摘した。